Jellemzői veleszületett immunitás - szól az állattenyésztés
A veleszületett immunitás jellemzi például az örökölt, Ebben a tekintetben meg függetlenül működik jelenlétében genetikai elemek az idegen testet és közvetíti számos tényező - a fizikai, kémiai, humorális és celluláris. Veleszületett immunrendszer sejtek (monociták / makrofágok, dendritikus sejtek, természetes killer-sejtek, granulociták) nincs klasszikus antigén-felismerő receptorok, amely lehetővé teszi, hogy felismerje az egyedi epitópok antigén és nem képeznek memória idegen elején. Ezek azonban nem ismeri fel a receptor révén speciális struktúrák (minták) a csoport a molekula, amely jellemzi a teljes molekuláris mozaik kórokozó. Ez a felismerés kíséri gyors sejtjeinek aktiválását, meghatározzuk a képességet és hajlandóságot végrehajtja a védelmi effektor funkciókat. Azonban ezek az eljárások lényegesen különböznek azoktól, amelyek fejlesztése során a kialakulását az adaptív immunitás. Aktiválása veleszületett immuneffektorok végezzük eredményeként a közvetlen külföldi fellépés kezdődő ezek receptorai, ami nem igényel a fejlesztés folyamatainak celluláris kölcsönhatások, tenyésztési és érését effektor sejtek. Ezzel szemben a veleszületett immunrendszer adaptív immunitás fejlesztése nélkül ezek a folyamatok nem alakul ki. Egyik fontos következménye veleszületett immunitás a faj ellenállás (immunitás) külön fertőzések. Mivel immunitás definíció nem lehet nem-specifikus, és a már elavult használt szinonim veleszületett immunitás az a „nem-specifikus immunitás» (Nem-specifikus immunitás).
Az adaptív immunrendszer alapvetően eltér a veleszületett. Adaptív immunitás az egyetlen formája vékony-specifikus védelmi elleni genetikai idegenségét széles, nem öröklődik, csak akkor képződik jelenlétében genetikailag idegen antigének által közvetített humorális és celluláris faktorok. Cellular tényezők kifejezni adaptív immunitás (hajtjuk a felületen) en tigenraspoznayuschie receptorok és a forma egy memória idegen elején, amellyel érintkezésbe kerülnek. Mint már említettük, a szükséges mechanizmusokat adaptív immunitás a folyamatok a celluláris kölcsönhatások, reprodukciós elődei effektor sejtek és azok differenciálódását. Alapvető különbségek veleszületett és szerzett (adaptív) immunitás táblázatban mutatjuk be. 8.1.

Védő faktorok veleszületett immunitás vannak osztva két fő csoportba (lapon. 8.2). Egyikük - a „tényezők természetes vagy veleszületett rezisztencia”, a kialakulását és működését, amely független a lenyelés idegen antigének, egy antigén szerkezetét vagy formája az anyag. Sőt, ezek a tényezők nem aktiválódnak hatása alatt antigének. Valójában, ilyen tényezők fiziológiai gát, amely megvédi a testet a antigén agresszió. Munkájukat az egész az ő fertőzések leküzdésében, de a legnagyobb hatékonyságot a tényezőket mutatja be az első 3-4 óra után a szervezet fertőzés. Ez elsősorban fizikai és kémiai tényezők. Ezek nincsenek hatással a kialakulását az adaptív immunitás.

Egy másik csoport a tényezők veleszületett immunitás - a „tényezők alakításában folyamat doimmunnogo gyulladást.” Ezek képviselik humorális és celluláris faktorok, amelyek szintén kialakítva, és függetlenül működnek a lenyelés idegen antigének, de lehet aktiválni akció keretében, és ezek hatása mind a létrejövő specifikus adaptív immunválasz és a funkcióját. Ezek a tényezők is hatnak az egész szervezetben a fertőzések leküzdésében, de a legnagyobb hatékonyságot után megfigyelt 72-96 órával a fertőzés után. A folyamatokat doimmunnogo gyulladás és egyúttal képező korai indukálható válasz ezekre a tényezőkre, és a kaszkád fejlődő védőválaszokkal veleszületett immunitás lokalizálni mikroorganizmusok a gyulladást, megakadályozzák elterjedése révén a szervezet felszívja, és megölik őket. Recycling részecskék adszorbeált antigént és az antigén-prezentáló őket iniciátorok adaptív immunitást, celluláris faktorok a veleszületett immunitás az alapot, amelyre van kialakítva egy meghatározott adaptív immunválasz, azaz a immunitás második védelmi vonalat. Emellett részt vesz a reakciók az adaptív immunrendszer, ezek a tényezők növelik annak hatékonyságát. A fő különbség ezen tényezők táblázatban mutatjuk be. 8.2.
Mint már említettük, a kialakulását speciális vezető immunválasz befejezése védekezési reakciók, hogy a megsemmisítése az antigén és kiválasztás a szervezetből. Ezt kíséri a befejezése gyulladás.
Leírja a tényezők a veleszületett immunitás, meg kell jegyezni, jellemző e többkomponensű, különböző szöveti lokalizáció, genetikailag ellenőrzött egyéni szinten.
Általában ezek a folyamatok végrehajtása a szervezet válasza a bármilyen antigén. Azonban a részvételének mértéke, súlyossága és hatékonyságát határozza meg több paramétert. Köztük van a fő jellemzői az antigén szerkezetét, a jellege belép a test (a penetráció a mikroba keresztül a sérült bőrön vagy nyálkahártyán, sejt transzplantáció, szövet vagy szerv, intradermális, intramuszkuláris vagy intravénás injekció formájában rendezi oldható vagy korpuszkuláris antigének és mtsai.), A genetikai nyomon követi, reaktivitás.
Az egyik erőssége indukálására gyulladás kialakulásával faktorok aktiválásával komponensek mikroorganizmusok magukat, mint a lipopoliszacharid (LPS) a Gram-negatív baktériumok, lipoteikolsav Gram-pozitív baktériumok, peptidoglikán a Gram-negatív és Gram-pozitív baktériumok, a minimális összetevő olyan muramil-dipeptid, mannánok, bakteriális DNS, kettős szálú RNS-vírusok, gombás glükánok és mtsai. elismerése e struktúrák rezidens makrofágok kíséri aktiválása celluláris faktorok vrozhdennog Az immunitás és indukciós a gyulladásos válasz. Más termékek, aktiváló celluláris komponensek a veleszületett immunitást, beleértve a endoteliális sejtek a kis vérerek, a hatása a komponens (hisztamin, trombin, az IL-1, TNF # 945; és mtsai.), által termelt szöveti károsodás a bevezetése a mikroba.
Egy erős tényezője a gyulladás kialakulásával doimmunnogo az későbbi makrofágok aktiválása gyulladásos izzadmány mozgó érési vér keringő monociták és részt vesz a gyulladásos hangsúly. Aktiválása fagociták nem csak elismerést idegen részecskéket, antigén befogó és felszívódása, hanem eredményeként fellépő ezen folyamatok kialakulását és szekrécióját oldható termékek - citokinek. A szekretált citokinek, bakteriális komponensek, szöveti károsodás termékek aktiválják az endotél sejtek a kapillárisok egy lapos részesülő nagy alakja (köbös) endothelium. Aktiválása az endoteliális sejtek kíséri szintézise és szekréciója a citokinek, kemokinek elsődlegesen tulajdonságait mutatják szükséges kemoattraktáns és diapedézist (infiltráció) a leukociták a falon keresztül a véredény a kandalló kialakított gyulladás. Az eredmény a fejlesztés a helyi vaszkuláris reakció, az alapvető lépéseket, amelyek közé tartoznak:
• az eredeti rövid távú (néhány másodperc és néhány perc) lassulása a véráramlás, végeredményben bővíteni szöveti sérülés és a kialakulása a gyulladásos mediátorok;
• következő amplifikációs kapilláris falán permeabilitás és értágulás, megnövekedett vér és nyirok áramlását, szállítása plazmafehérjék, a kivándorlás leukociták a véráramból a gyulladásos fókusz, fokozott szekréció citokinek gyulladásos sejtek, kialakulását lokális ödéma és a vérbőséget aktív;
• erősítés a gyulladásos izzadmányban impregnált szövet, az átalakítás a fibrinogén hatása által citokinek a fibrinhálózat amely thrombosing a nyirokrendszeren és megakadályozza a mikrobák helyi terjedt túl a gyulladásos fókuszt. Ezt segíti elő a fokozatos változásának a megnövekedett vér áramlását a kialakulását a vénás pangást thrombosis venulák nyújtó demarkációs gyulladásos fókuszt a környező szöveteket. Vannak klasszikus gyulladás jeleit - duzzanat, bőrpír, fájdalom, láz, láz, és segít megtisztítani a szervezetet a gyulladás által kiváltott mikroflóra.
A kivándorlás leukociták a véredény a szövetbe (diapedézist)
A folyamat a sejtek vándorlását a véredények útján a vascularis endothelium a szövetet nevezzük diapedézist. Ez a legfontosabb a reakció, amellyel a sejtek képesek migrálni területeken károsodott szövetek és így a hangsúly a gyulladás a lokalizáció a kórokozó, és megsemmisíti azt. diapedézist folyamatot szemlélteti az alábbi példája neutrofilek (ábra. 8.1).
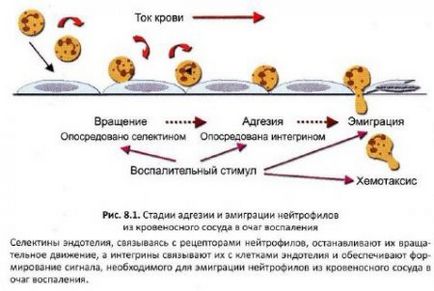
A kezdeti szakaszban a ezt a folyamatot az jellemzi, neutrofil mozgása marginális gördülő (gördülő-hatás) mentén a kis vérerek felszínén érintetlen belhámsejtek. A kölcsönhatás ezen sejtek endothelialis sejtekben adhéziós molekulák (P-szelektin, CD62P), megjelenő endoteliális sejtek befolyása alatt baktériumok vagy termékek sérült szövet. Jellemzően, egy P-szelektin lévő sejtek a pelletek, de az aktiválás mozgatjuk felületén a membrán. Kölcsönhatás a P-szelektin a fagocita membrán adhéziós molekulák - L-szelektin (CD62L) - egy alacsony affinitású (alacsony szilárdságú), mint az L-szelektin könnyen rétegesen a membrán elasztáz. Ezért, neutrofil továbbra roll mentén endoteliális sejtek a véredény, de a sebesség csökken.
Teljes stop motion neutrofil képződése jellemzi a második lépésben a tapadás miatt a váladék a endoteliális sejtek lipid - vérlemezke-aktiváló faktor - PAF (vérlemezke-aktiváló faktor). Ez a tényező aktiválja a neutrofileket, valamint indukálja a felületi expresszióját a integrin CD11a / CD18, egy antigén ismert, mint LFA-1 (limfocita funkcióval összefüggő antigén-1, a ragasztó antigén 1. típusú limfocita funkció-asszociált). Azalatt történt konformációs változások neutrofil membránok biztosíthatja a megnövekedett affinitás a receptor a ligandum, ICAM-1 (CD54), endothelialis sejtjei expresszálják. Integrin CD11a / CD18-cal (LFA-1) szintén kötődik az ICAM-2-ligandum endoteliális sejtek (CD102), de ez a membrán glikoprotein expresszálódik túlnyomórészt nyugvó endoteliális sejtekben. Tapadás a neutrofilek endoteliális sejtekhez növeli ligandum PSGL-1 mieloid sejtek (P-szelektin glikoprotein ligand-1) vagy SELPLG (szelektin P ligandum) - CD162, kötődik a P-szelektin endoteliális sejtek. Kölcsönhatás a ligandum-receptor kölcsönhatás stabilizálja a neutrofilek endoteliális sejtekhez, neutrofil húz pseudopodiás, és használja őket, hogy vándorolnak a belhámsejtek között a véredény a szövetbe. Receptorok és ligandumok a neutrofil kötődést, amely meghatározza a folyamat a kivándorlás a neutrofileket a véredény és a hangsúly a gyulladás ábrán mutatjuk be. 8.2
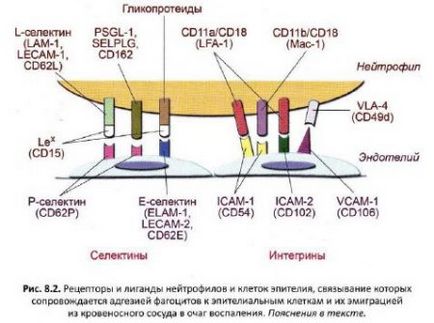
A folyamat során a kivándorlás a neutrofileket véredények fontosak által kiválasztott citokinek aktivált makrofágok, endothelialis sejtek és maguk a neutrofilek is. IL-1 vagy TNF # 945;, makrofágok által termelt, endoteliális sejteket aktiválódik, és indukálódik, hogy kifejezze az E-szelektin (CD62E), leukociták kötődését glikoproteinek és növeli sejtadhéziót. Mivel a szelektin szénhidrát-kötő fehérjék, azok kölcsönhatása membrán glikoproteinek keresztül végén szénhidrát elágazó (triszacharid) - szialil Lewis (Le, CD15), egy része a glikolipidek és glikoproteinek a sejtmembrán. Hatása alatt az IL-1 szintén fokozott termelését az IL-8 által endoteliális sejtek, amelyek kemotaktikus tulajdonságokat, és elősegíti a migráció új neutrofilek a gyulladásos hangsúly. TNF # 945; stimulálja az IL-1 az endoteliális sejtek, fokozza a kibontakozó reakció Végső soron ez fokozza a gyulladásos folyamatot, ami a vazodilyatsii, fokozza prokoaguláns aktivitását, trombózis, megnövekedett adhéziós fehérjék, és a termelés a kemotaktikus faktorok.
Átállítása a gyulladásos fókuszt perifériás vérből monociták és neutrofilek fagocitáiják végrehajtása és a tenyésztés a baktériumok, valamint a megsemmisítése a sejtek a sérült szövet és haldokló sejtek a gyulladás kialakulásával. A monociták differenciálódtak makrofágok számát megszorozzák a fagocita sejtek a gyulladásos fókusz és fenntartása a különböző szekretált citokinek különböző tulajdonságok, beleértve a baktericid. Amikor egy hatalmas fertőzés a gyulladásos gócokat képződött gennyes tömege, maradékként tartalmazó szövet, élő és elpusztult fehérvérsejtek, élő és elpusztult baktériumok, a maradék a fibrin, nyirok, a szérum.
Meg kell jegyezni, hogy a természet a doimmunnogo gyulladás és annak kifejezése nagyban meghatározza a természet a hívó a mikroorganizmus. Így, amikor fertőzött gombák és mycobacteriumok organizmus folyamatok kidolgozása granulómás gyulladása, bélféreg parazita és allergén hatások gyulladás kísér infiltrációval együtt a sérült szövet preferenciális eozinofil tartományban bakteriális fertőzések, például, lizozim rezisztens Gram-pozitív baktériumok, indukálja fejlesztése akut gyulladásos válasz nélkül maradandó szövetkárosodást. A kábítószerek használata elősegíti a takarítást és a gyógyulás a gyulladás hangsúly.