Savas és lúgos akkumulátorok
Az akkumulátor kémiai áramforrás, amely képes felhalmozni, és tartsa egy ideig a villamos energia és a szükséges, hogy ez a külső áramkörben.
Az akkumulátor önmagában nem termel villamos energiát. Ez csak akkor halmozódik ellenében: áramátmenettel külső forrásból származó kíséri átalakítása villamos energia kémiai energiává, ennek eredményeként az akkumulátor is lesz forrása a jelenlegi.
Amikor az akkumulátor lemerül tárolt elektromos energia fogy a külső áramkörben kapcsolódik hozzá (a kémiai energia alakul át elektromos áram).
A megfelelő működéshez az akkumulátor ellenáll több száz cikluson feltöltési és kisütési.
Attól függően, hogy a készítmény az elektrolit különböztethető:
· És az alkáli elemek.
A legegyszerűbb sav akkumulátor két ólom merített elektródák kénsav oldat.
A folyamatok zajlanak a sav akkumulátor, leírható a következő egyenlet szerint:
PbSO4 - ólom-szulfát (ólom-szulfát).
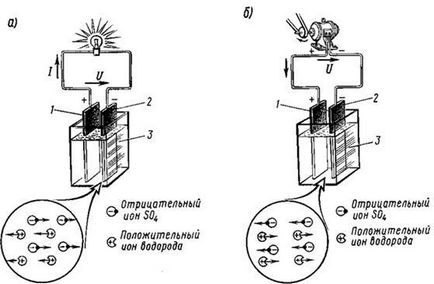
4.2 ábra. Áthaladás elektrolit a pozitív és negatív ionok a) és b kisülési) akkumulátor töltési savat
Mozdonyon és a vonaton a legszélesebb körben használt alkáli elem (sokkal hosszabb az élettartama, mint a sav).
A teljesen feltöltött akkumulátor EMF körülbelül 2,2 V, megközelítőleg azonos feszültség a kivezetései, mivel a belső ellenállás nagyon kicsi.
Amikor a kisülési feszültség gyorsan esik 1,8-1,7 V, a kisülési feszültség leállítjuk károsodásának megelőzése.
A leggyakoribb a nikkel-vas (VAW) és a nikkel-kadmium (NC) akkumulátorok alkáli. Az ilyen és más aktív anyaggal a pozitív elektród a töltött állapotban áll a nikkel-hidroxid NiOOH, amelyhez hozzáadjuk a grafit és a bárium-oxid.
Grafit növeli az elektromos vezetőképessége az aktív tömeg, és a bárium-oxid - élet. Az aktív tömegét a negatív elektród a nikkel-vas akkumulátor áll vasport az adalékanyagokkal, és a nikkel-kadmium elemek keverékéből kadmium és vasport. Az elektrolit oldat káliumhidroxid hozzákeverésével monohidrát lítium ami növeli az akkumulátor élettartamát.
Elektrokémiai reakciók során előforduló töltési és kisütési az alkáli elem lehet, amelyet a következő egyenlet:
2Ni (OOH) + 2KOH + Fe 2Ni (OH) 2 + 2KOH + Fe (OH) 2
2Ni (OOH) + 2KOH + CD 2Ni (OH) 2 + 2KOH + Cd (OH) 2
Ni (OOH) - nikkel-oxid-hidrát;
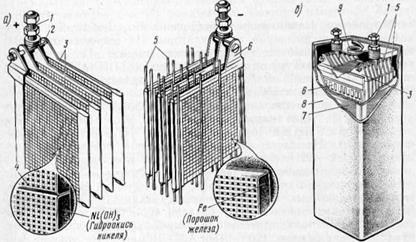
4.3 ábra. Semiblocks negatív és pozitív lemezek (a) és az általános nézet (b)
nikkel-vas akkumulátor TPNZH alkalmazott mozdonyok:
1 - pin-out; 2 - Stud; 3 - pozitív lemezek; 4 - acél nikelerovannye keret (lamella); 5 - szeparátorok; 6 - negatív lemezek; 7 - egy házat;
8 - gumi fedlappal; 9 - a dugóval lyuk elektrolit töltési
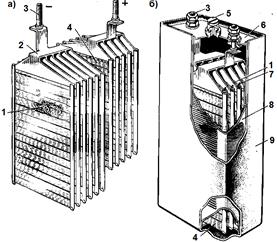
Ábra 4.4. Semiblocks pozitív és negatív lemezek (a) és perspektivikus nézetben (b) nikkel-kadmium akkumulátort ICH 100 e.p.s. 1 - negatív lemezek; 2 - egy összekötő híd; 3 - a vezető pin; 4 - pozitív lemezek; 5 - furat dugóval az elektrolit; 6 - burkolat; 7 - elválasztó; 8 - egy házat; 9 - gumihüvelyből
A teljesen feltöltött akkumulátor EMF mintegy 1,45 V. A nagy belső ellenállása feszültség mentesítési, lényegesen kisebb, mint ez az érték. Amikor a kisülési feszültség gyorsan esik 1,3 V, majd lassan, hogy teljesíti az 1 V alatti feszültséget tilos.
Előnyei alkáli elemek:
· Ennek gyártása ne használjon szűkös vezet;
· Rendelkeznek nagyobb mechanikai erőt és kitartást, nem fél az erős kisütőáramok, remegés, ütéseket és még rövidzárlat;
· A hosszan tartó inaktivitás kis veszteségek önkisülés, és nem megy rosszul, hosszú élettartam;
· A működés során bocsátanak ki minimális mennyiségű káros gázok és gőzök;
· Könnyebbek;
· Kevésbé igényes, tekintettel a tartós szakképzett ellátást.
· Alsó hatékonyság
· Drágább.
1. Mi a célja az akkumulátor?
2. A működési elve az akkumulátor sav.
3. Az elv a alkáli elem.
4. Az előnyök alkáli elemet.
5. hátrányai alkáli elemet.
6. Mi az EMF A teljesen feltöltött akkumulátor?
7. Mi a legegyszerűbb savas akkumulátor?
8. Hogyan olyan eszközök, amelyek átalakítani a kémiai energiát elektromos energiává?
9. Mi az elektrolit?
10. Mi az elektrolízis?
11. mely részei a molekula szétesik kénsav?
12. Mi a galvánelem Volta?
13. Hogyan történik a polarizáció elem?
14. Milyen hatással van a hidrogén ionok akkumulátor munka?
15. Mi a száraz galvánelem?
16. Milyen az elektromos áram a folyékony vezetékek?
17. Mi a tervezési-savas akkumulátorok?
19. Hogyan tölteni az akkumulátort?
20. Mi a jele a végén a töltés az akkumulátor sav?
21. Ennek jeleként a végén a töltés alkáli elem?
22. Hogyan lehet csatlakozni az elemeket az elem?
4.3. Módjai elemeket az akkumulátor
Következetes. ha minden egyes mínusz korábbi forrás csatlakozik a későbbi előny. Szerint a második törvénye Kirchhoff kapott EMF összegével egyenlő az EMF egyes elemeket. A nagyobb akkumulátor a lánc, annál több a feszültség a vevők.
Ha az akkumulátor rövidre a külső R ellenállás, akkor
Elemek sorba kapcsolt, amikor a fogyasztó akkumulátor feszültsége felett feszültség.
Párhuzamos. amikor a pozitív pólusok akkumulátorok több összekapcsolt és kimenetre a teljes plusz és negatív pólusát összekapcsolnak és kibocsát egy közös hátránya.
Ábra 4.5. Az alkalmazott feszültség a vevő, különböző számú sorba kapcsolt akkumulátorok
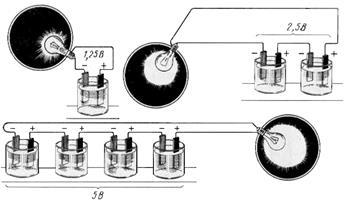
Párhuzamos kapcsolat használata, ha a feszültség egyenlő a feszültség a fogyasztó akkumulátor, valamint a szükséges áram a fogyasztó által nagyobb kisülési áram az akkumulátort.
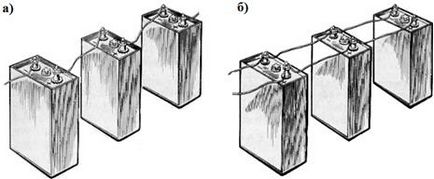
Ábra 4.6. Szekvenciális (a) és párhuzamos (b) egy vegyületet, akkumulátorok
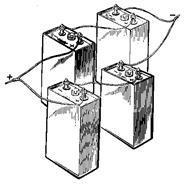
A kevert vegyületet alkalmazunk, amikor az elemeket nem biztosítják a lehetőséget, hogy megszerezze a szükséges áram és feszültség. Ábra. 4.7 mindegyikében két párhuzamos akkumulátor csoportok két sorba kapcsolt akkumulátor.
4.7 ábra. Vegyes vegyületet akkumulátorok
Az akkumulátorok a legtöbb esetben áll sorba kapcsolt elemeket. Vegyes és párhuzamos kapcsolása elemek ritkán használják, mert nehéz biztosítani egységes jelenlegi elosztása a párhuzamos ágak.
1. Milyen kapcsolat az akkumulátor tudja?
2. Melyek az akkumulátor soros kapcsolat?
3. Mi a kapcsolat az akkumulátor nevezzük párhuzamos?
4. Mi a kapcsolat az elemek az úgynevezett vegyes?