Ózon (kémiai elem) tulajdonságok képletű kijelölése
Rendkívül értékes az egész emberiség tulajdonságait egy gázt, mint az ózon. Element, amelyben ki van alakítva, - oxigén O. Tény, az ózon O3 - az egyik allotrop módosítások oxigénellátását három egységből áll a Képlettároló (O ÷ O ÷ G). Egy első és egy ismert vegyület - önmagában oxigéngáz éppen az, hogy van kialakítva két atom (D = O) - O2.

Allotrópia - képes egy kémiai elem képez számos különböző tulajdonságainak egyszerű vegyületek. Köszönhetően az emberiség, és megvizsgálják anyagok, mint a gyémánt, és a grafit, monoklin és rombos kén-, oxigénatom, és az ózon. Elemet tartalmaz, ilyen képesség nem feltétlenül korlátozódik csupán két módosítást, néhány közülük.
A felfedezések története vegyületek
Az összetevő egység számos szerves és szervetlen anyagok, beleértve például az ózonréteg - egy kémiai elem, amelynek szimbóluma O - Oxigén, görög «oxys» - savanyú, és a «gignomai» - szülni.
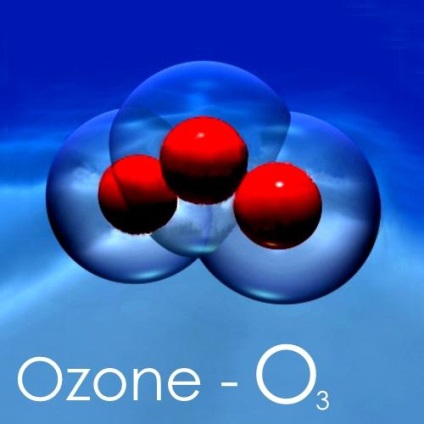
elektronikus szerkezet
Az azonos szerkezeti fragmens O2 és O3 - egy kémiai elem. Az ózon egy bonyolultabb szerkezet. Az oxigén még mindig egyszerű - két atom oxigénnel csatlakozott egy kettős kötést tartalmazó, és a ϭ- π-komponens szerint a vegyértéke az elem. O3 több rezonáns struktúrákat.
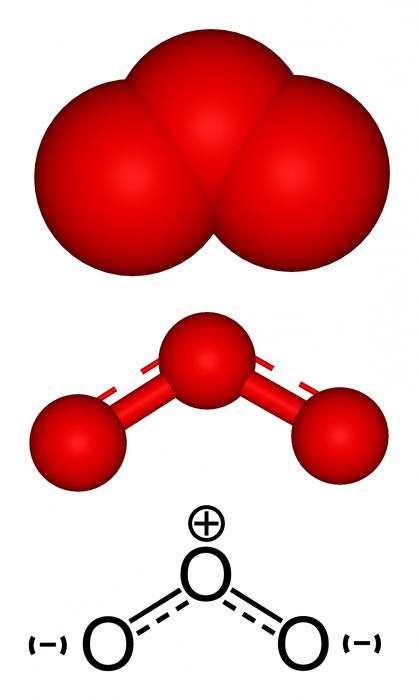
szintézis módszerek
A formáció egy gáz, például ózon, egy kémiai elem oxigén kell lennie egy gáznemű közeg formájában egyes atomok. Az ilyen körülmények között jönnek létre ütközések O2 oxigén molekulák elektronokkal során elektromos kisülést, vagy egyéb részecskék nagy energiájú, és amikor ezt besugározzuk ultraibolya fény.
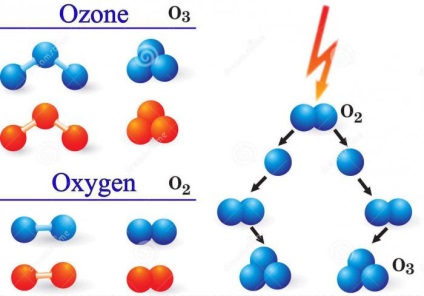
A oroszlánrészét a teljes mennyiségű ózon által termelt fotokémiai úton a természetes atmoszferikus körülmények között. Az emberek szívesebben használják a kémiai aktivitását más módszerek, mint például, elektrolitikus szintézist. Ez abban áll, hogy a vizes elektrolit közegben platina elektródát helyezünk, és hagyjuk a jelenlegi. A reakcióvázlat:
fizikai tulajdonságok
Oxigén (O) - egységet komponens, így például ózon anyag - kémiai elem, amelynek általános képletű és a relatív moláris tömegű felsorolása a periódusos. Képző O3. Oxigén szerez tulajdonságai gyökeresen eltérő tulajdonságait O2.
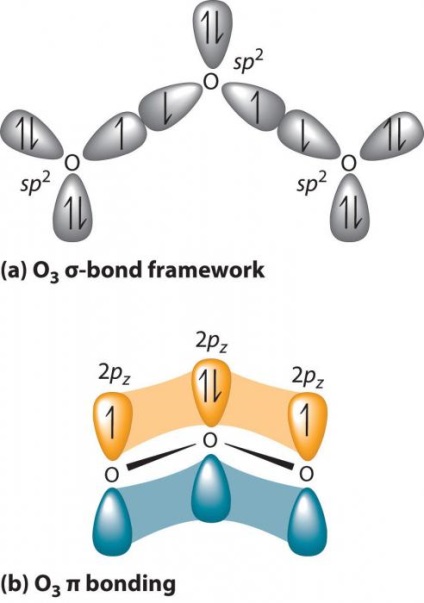
Gáz kék - ez egy közös állam ilyen vegyületek például az ózon. Kémiai elem képlet mennyiségi jellemzőit - az összes meghatározott azonosítási és az anyag vizsgálata során. A forráspont neki -111,9 ° C, folyékony állapotban van egy sötét lila színű, míg a további csökkentése mértékben -197,2 ° C olvadáspontú kezdődik. A szilárd halmazállapotban ózon válik fekete színű, lila árnyalat. Oldhatósága tízszer magasabb, mint az O2 oxigén tulajdon. Amikor a legtöbb kis koncentrációja a levegőben a szaga ózon, mégis éles, konkrét és hasonlít a szaga fém.
kémiai tulajdonságok
Nagyon aktív, a reakció szempontjából, a gáz az ózon. Kémiai elem, hogy ez képezi - jelentése oxigénatom. Jellemzői, hogy meghatározzák a viselkedését a ózon a kölcsönhatást más anyagokkal, - magas oxidáló képessége és instabilitása maga a gáz. Magas hőmérsékleten, bomlik példátlan mértéke, felgyorsítja a folyamatot, és katalizátorok, például fém-oxidok, klór, nitrogén-dioxid, és mások. Ózon oxidáns tulajdonságok miatt jellemző tulajdonságok molekuláris szerkezete és a mobilitása egyik oxigenizáció alkilcsoport, amely lehasad alakul át oxigéngázt: O2 + O3 → O ·
Oxigén (építőelem, ahonnan az épített molekula anyagokat, mint például oxigén és ózon) - kémiai elem. Amint meg van írva az egyenleteket reakció - Körülbelül ·. Az ózon oxidálja a minden fém a arany, platina és alcsoportjai. Reakcióba lép a gázok légköri - kén-oxidok, nitrogén-és mások. Nem maradnak inert és szerves anyagok, különösen gyorsan folyamatok diszkontinuitások többszörös kötések képződése útján közbenső vegyületek. Rendkívül fontos, hogy a reakció termékei ártalmatlan a környezetre és az emberekre. Ez a víz, az oxigén, a magasabb oxidok különböző elemeinek, a szén oxidjai. Reakció ózonnal nem jön bináris vegyületek kalcium, titán és szilícium oxigénnel.

kérelem
A fő terület, ahol használt „rossz szagú” gáz - ez ozonation. Az ilyen sterilizálás módja sokkal hatékonyabb és biztonságosabb, mint az élő szervezetek klóros fertőtlenítés. Amikor vizet tisztítunk, ózonnal képződés játszódik toxikus származékai metán veszélyes halogénatommal szubsztituált.
Mindez egyre ökológiai sterilizálási módszert használják az élelmiszeriparban. Ózon kezelt hűtőberendezések tárolására szolgáló termékek segít neki elvégezni a eltávolítása szagokat.
Az orvosi fertőtlenítő tulajdonságai ózon szintén nélkülözhetetlen. Ezek fertőtlenítse a sebet, sóoldat. Ozonated vénás vért, valamint a „szagú” gáz kezelésére számos krónikus betegség.
Mivel a természetben és az érték
Egyszerű anyag ózon - elem gáz összetételét sztratoszféra közeli régióban térben helyezkedik el a parttól mintegy 20-30 km-re a felületre. Fenti vegyület izolálását során fordul elő a kapcsolódó folyamatok az elektromos kisülések, a hegesztés során, a másoló berendezést. De a sztratoszférában van kialakítva, és tartalmaz 99% a teljes ózon mennyisége jelen van a Föld légkörébe.
Vital bizonyult a gáz jelenléte a Föld-közeli helyet. Ez képezi az ott egy úgynevezett ózonréteget, amely megvédi minden élet a letális ultraibolya napsugárzás. Furcsa módon, de egy par egy óriási előnye, maga a gáz veszélyes az emberre. Koncentrációjának növelése az ózon a levegőben légzés személy káros a szervezetre, mert az extrém reaktivitása.

Miért utaskísérők soha ne igyon teát és kávét a levegőben? Láttál egy légiutas-kísérő látta a repülőgép fedélzetén teát vagy kávét? Megvan a saját oka.

