Lehetséges negatív - hivatkozási vegyész 21
Kémia és Vegyészmérnöki
erőtér időben állandó úgynevezett konzervatív, ha ez ad egy skalár értékű függvény F = F x, y, z) - potenciális, a negatív gradiens, amely kényszeríteni [c.123]
Hasonló helyzet figyelhető meg abban az esetben, kadmium, azon a tényen alapul, hogy ez vonatkozik a filmmel CC1 (0H) 2 (PR = 2-10). A számított potenciál -0.54 V és pozitív képest a lehetséges a vas, míg a tényleges potenciális negatívabb, mint a vas (lásd. 3.3.). A megfigyelt potenciális több negatív kadmium, valószínűleg az ismert hajlama CC1 + ionok komplexet képeznek. Sd amely csökkenti ion aktivitása alacsonyabb értékre. mint a megfelelő telített C oldatot (1 0H). - megjegyzés. aut [c.226]
Hatása az összeg a monovalens ionok -potential negatív töltésű kollódiumban membránok lehet szemléltetni az adatok 3. P. Kozmina kapott 0,001 n. oldatok alkálifém-kloridok (ábra. 96). A két vegyértékű ionok releváns adatokat ábrán szemléltetjük. 94. [c.157]
A mennyiség q nevezett csereáram (pontosabban a csereáramsűrűség). Ha a potenciál negatívabb, mint az egyensúlyi, majd a [c.217]
E ° 2 -... Az elektród potenciál kevesebb algebrai mennyiség (kiszámításakor az EMF az elektrokémiai cella vett képessége kevesebb, algebrai érték szerinti XIV-2 asztal, kivonjuk a lehetséges egy nagyobb algebrai értéket más szóval, a potenciális pozitív pólusát az elektrokémiai elem vonjuk potenciális negatív pólus). [C.325]
A fém lerakódás. ezüst, amelynek több negatív potenciál (ólom, kadmium, cink) kell alkalmazni, vagy a higany összeolvadt platina elektród. Abban az esetben, platina elektród egyidejűleg a lerakódást a fém felszabadul hidrogénatom. [C.64]
Ha a potenciál negatívabb, mint az egyensúlyi, majd 1k> 1 a rendszerben és a katód áram folyik. Ha f> fr, akkor n> (a rendszerben, és az anód áram folyik. Használatával az Arrhenius-egyenlet. Kifejezések a K és a következőképpen írható fel (elhanyagolva adszorpciós g () 1-potenciál) [C.10]
A oxidáló ereje a vízben oldott oxigén sokkal aktívabb hidrogén ionok, és ezért a víz tartalmazó oxigén jobban veszélyes korróziós otnoscheniya. Korrózió amplifikált n növelésével hidrogénionok koncentrációját az oldatban. Felületi valós fémek és ötvözetek általában heterogén, néhány részletben különböznek elektród potenciálját. Ennek eredményeként, korrózió következik be azon részeit a fém, ahol a potenciális negatív. [C.148]
Korrózió hidrogénnel depolarizációval jellemző fémek. amelynek több negatív elektród potenciálja nem hidrogénatom, és továbblépünk általában savas közegben. Azonban, számos aktív fémeket. például magnézium és annak ötvözetei korrodálja azonos módon semleges és lúgos közegben miatt a hidrogén feltárását a vízmolekulák reagáltatásával [c.35]
Működés közben a terhelés az elektrokémiai cella, azaz. E. körülmények között, ahol a pozitív és negatív elektródák vannak csatlakoztatva egy külső áramkörbe. amelyen keresztül egy aktuális (ohm, ábra. 1), az elektród potenciál eltolják az egyensúlyi érték. Az elektronok haladnak át egy külső áramkör negatív a pozitív elektród, míg a negatív elektród potenciál válik pozitív (vagy kevésbé negatív). A pozitív elektród potenciálja válik negatív (vagy kevésbé pozitív). Néhány elektróda eltolódás lehetséges az egyensúlyi érték egy kis érték. Például, a cink-elektróda egy ilyen váltás általában 0,05-0,2 B, [C.20]
Ábra. VII, 12. függés -potential negatív töltésű részecskék agyag, a sugara számláló l
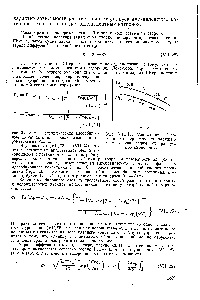
Abban az esetben, szerves depolarizátor. Nem kell a díjat, a fő tényező. befolyásoló könnyű való visszanyerését, ez a változás g) -potential. Ez abban nyilvánul meg, egy kellően tiszta formában. ha a hordozó elektrolit áll egyszeres töltésű ionok (hiányában specifikus adszorpció és ezek hatása a pH-csökkenés folyamat). Ezért, amikor. növekvő koncentrációjának a hordozó elektrolit abszolút értéke z) -potential negatív elektród ennek megfelelően csökken, a hasznosítási arány növekszik töltetlen szerves molekulák, azaz. e. 1/2 felé tolódott kevésbé negatív értékei potenciálok. [C.14]
Az úgynevezett Elektrokinetikus ioteitspalom Milyen tényezők g.lpyagat a lehetséges megváltoztatásának lehetőségeit negatívan Ami [) I / ksiiyh chastnts amikor be a szol kálium-nitrát. BA [) és lantán la [c.103]
Valamennyi fent világossá válik, hogy miért képes tömöríteni egy elektromos kettős réteg és hogy csökkentsék a g-poten-tial növekedése számos kationok a Li + s +, és az anionoknak a sorozat p 1. ábrán. VII, látható 12 és Jenny talált Reytemeye beállított függőség -potential negatívan töltött részecskéket az agyag vizes szuszpenziót telített különböző egy- és kétvegyértékű ellenionok, a mérete az ionok. Mint látható, [c.186]
A lantanidák - erős redukáló a potenciális negatív elektród, és változik -2.4 a -2.1 a. Ezek bomlanak víz (előnyösen melegítés), és könnyen reagálnak savakkal képeznek sókat háromértékű elemek. A helyreállító Activity esik cérium a lutécium. Ezek könnyen oxidálódik oxigénatom, az első három elem a szokásos hőmérsékleten. és a többi melegítéssel. Ennél a rea-to-CIÓ kinyúló megjelenése nagy mennyiségű hőt, jellemzően oxidok keletkeznek, és D. a készítmény Me cérium, prazeodímium és terbiummal van oxidálva SeOa, RgvO és T40. Oxidjai lantanidák alapvető oxidokat. Ezek erőteljesen egyesítik, vízzel reagáltatjuk, hidroxidok, azzal jellemezve, hogy vízben való oldhatósága alacsony. Ezeket úgy állíthatjuk elő, kicserélési reakciói lantanida sókat erős lúgok. A fő karakter esik hidroxidok Ce (OH) egy Lu (OH) z kapcsolatban csökkentése ferriion sugár (lantanida tömörítés). A hidroxidok utóbbi két elemet rendelkeznek gyengén ejtik amfoter jellegű. [C.334]
Elektromotoros SIPA (pl. Q. S.) Elektrokémiai áramkör által meghatározott legnagyobb potenciális különbség a pozitív és negatív elektródák. Az elektrokémiai reakció játszódik addig. míg ez a különbség. A reakció során, a negatív elektród potenciálja eltolódik a pozitív oldalon, és a pozitív - negatív. Amikor a potenciálok az elektródák egy vonalba kerülnek, e. d. a. eltűnik, a rendszer jön n egyensúlyt a reakció leáll. Meg kell azonban megjegyezni, hogy van egy potenciális különbség az áramkörben előtt a zamosaniya rövid zampsaniya e mód. d. a. elektrokémiai áramkör nulla, mivel a potenciálok az elektródok miatt polarizációs lényegében azonosak. Ebben az üzemmódban az elektrokémiai reakció zajlik a leggyorsabban és a rendszer lehetővé teszi a maximális áram. [C.17]
A során Fizikai Chemistry Edition 3 (1975) - [c.573]