Következményei a törvény Raul
Tól Raoult-törvény két fontos következménye van:
1) Solutions forraljuk magasabb hőmérsékleten, mint a tiszta oldószer;
2) oldatot megfagy alacsonyabb hőmérsékleten, mint a tiszta oldószer.
Nézzük meg őket részletesebben.
Forráspont folyadék egy fizikai folyamat az átmenet a gáz halmazállapotú vagy gőz, ahol a gázbuborékok képződnek az egész folyadék térfogata.
A folyadék forrni kezd, amikor nyomás eenasyschennogo gőz egyenlővé válik a külső nyomást. Ha külső nyomás (például levegő) nem változik, és az egyén samazhidkost és kémiailag tiszta anyag, majd forralás nyitott edényben, melegítjük állandó hőmérsékleten lép fel egészen addig, amíg teljesen eltűnik folyadékfázis.
Így, légköri nyomáson egyenlő 101,325 psi, a forráspontja a tisztított (desztillált) vízzel 100 ° C-on vagy 373,16K.
Ha a H2 O, hogy feloldódjon bármely nem-illékony anyag, a nyomás annak telített gőz csökken. A kapott oldat forrt, szükséges, hogy melegítse azt egy hőmérséklete magasabb, mint 373,16K, hiszen Csak ilyen feltételek mellett, a telített gőz nyomás ismét megegyezik az atmoszferikus.
Fagyasztás vagy kristallizatsiyapredstavlyaet egy fizikai jelenség kíséri az átalakítás egy folyadékot egy szilárd anyagot kapunk. Sőt, kristályszerkezetek vannak kialakítva a teljes folyadék térfogatának.
Fagyasztási eljárás akkor kezdődik, amikor a nyomás a telített gőz a folyadék feletti egyenlővé válik a nyomás a telített gőz fenti szilárd kristályok formájában.
Ha a külső (légköri) nyomáson állandó marad azhidkost nem tartalmaz szennyeződéseket, majd lehűtjük a kristályosodási hőmérséklete a folyadék állandó marad mindaddig, amíg a folyékony fázis teljesen átalakul szilárd.
Légköri nyomáson a 101,325 kPa, desztillált víz megfagy át 0 ° C-on (273,16K). A nyomás a telített vízgőz jég és folyadék ebben az esetben egyenlő 613,3 Pa.
Ahhoz, hogy egy vizes oldatot 0 ° C-on a telített gőz nyomása kisebb, mint 613,3 Pa és változatlan marad jégre. Mártott jég elolvad gyorsan a kondenzáció miatt rajta túlzott mennyiségű gőzt.
Csak akkor, ha a hőmérsékletet csökkentjük ismét lehetséges, hogy kiegyenlítse a nyomás a telített gőz fölött a folyékony és a szilárd fázis és oka kristályosodási folyamat.
Empirikusan azt találtuk, hogy növeli a forrási hőmérsékletet (tkip.), És a hőmérséklet csökkentése zamerzaniyarastvora (tzam.) Összehasonlítva a tiszta oldószer egyenesen arányos a az oldott anyag koncentrációja molal. Matematikailag ez felírható a következőképpen:
gdem- molal kontsentratsiyarastvorennogo anyag; eik rendre ebullioskopicheskaya (lat.ebbulio- forráspontú) és oszmométerek (. görög "Krios" - hideg) állandók, amelyek értéke csak attól függ prirodyrastvoritelya (7. táblázat).
7. táblázat EbullioskopicheskieEi krioskopicheskieKkonstanty bizonyos oldószerek (deg / mol)
Ebullioskopicheskaya oszmométerek konstantyrastvoritelya és azt mutatják, hány fokkal povyshaetsyatemperatura forrási hőmérsékleten, és csökken zamerzaniyarastvora oldásával nyert az egy kilogramm oldószerben móljára nonelectrolyte (m = 1 mol / kg).
Annak meghatározására EiKsperva értékek empirikusan opredelyayutDtkip. iDtzam. nagyon híg oldatok (m<<1), а затем полученные данные пересчитывают или экстраполируют для растворов сm= 1 моль/кг.
EiKmozhno értékeket elméletileg számított felhasználásával aránya van't Hoff:
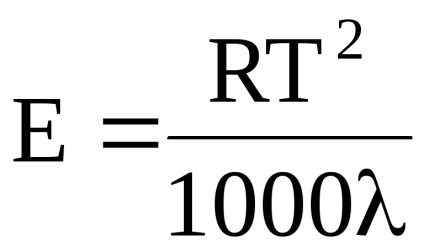
gdeR- egyetemes gázállandó; T- oldószer forráspontja közötti hőmérsékleten; - látens hője az oldószer elpárologtatása.
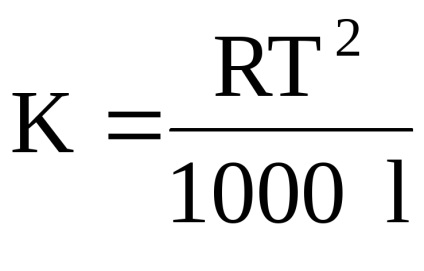
gdeT- hőmérséklet plavleniyarastvoritelya; l- plavleniyarastvoritelya fajhő.
Így, oldatok különböző jellegű anyagok, de ugyanakkor molal koncentráció forraljuk és fagyasztva egy és zhetemperature.
Figyelmet kell fordítani arra, hogy otlichierastvora a tiszta oldószer. Ha az utóbbi forr és megfagy postoyannoytemperature, torastvory csinálni intervaletemperatur, azaz során a forráspont hőmérséklete növekszik minden alkalommal, és ha megfagy - csökken. Ez annak a ténynek köszönhető, hogy az eltávolítása a folyadék fazyrastvoritelya például gőz vagy szilárd kristályok növeli a molal az oldat koncentrációját, mert oldott anyag a folyamat forrásban lévő, fagyasztás változatlan mennyiségben marad a folyékony fázisban (akár annak teljes forralás vagy fagyasztás), és a folyékony oldószer tömegének csökken.
A gyakorlatban izmereniyahtemperatury kipeniyarastvora fagyasztás vagy rögzíti a bekövetkeztének időpontját abban első szilárd kristályok (dlyatzam.) Vagy gázbuborékokat (dlyatkip.).
Lakásmegoldásban csökkenti a fagyasztási hőmérséklet lehetővé teszi, hogy használja őket, mint hűtőfolyadék.
Így, oldatok bizonyos szerves és szervetlen anyagokat használnak, mint fagyásgátló hűtésére a belső égésű motort, amikor azokat üzemeltető a különböző éghajlati viszonyok.
Ponizhenietemperatury zamerzaniyarastvorov elengedhetetlen az élő szervezetek. Így a saját sejtek, a folyadék olyan oldat különböző szervetlen és szerves anyagok. Egotemperatura fagyasztás alatt fekszik 0C (273,16K), így a sejtek nem pusztulnak el a feltételeket a hipotermia.
Ezen jelenség, a növények megmaradnak a téli hónapokban. Ezen túlmenően, minél nagyobb a az anyagok koncentrációjának a folyékony sejt, annál alacsonyabb a külső hőmérséklet hordozhatnak növény.
Sőt, csökkentő fagyáspontot az oldatot lehűtjük a sejtekben fokozott hidrolízisét nagyobb molekulatömegű, hogy a kis molekulasúlyú vegyületeket (például, szénhidrátok - akár glükóz).