Integrinek - studopediya
Továbbá leucin gazdag glikoproteinek a trombocita membrán ha van egy nagy kitüntetéssel adhéziós receptorok tartozó CE-Hi számára inshegrinov. Az integrinek - transzmembrán glikoproteinek Nye jellemzi általánosság
Stu proteinláncokkal antigén tulajdonságai és funkciói. Részt vesznek a kölcsönhatás-Corollárium sejt-sejt és sejt-mátrix subendotelial NYM. Mivel a képességét, az őszi kétirányú kommunikáció a számos fehérje integrinek tanítási-léteznek folyamatok felismerés, adhézió, instant-talkie a mátrix sejtek, reparatív, immun-kormányzati és egyéb reakciókat. A család integrinek receptorok fibrinogén, vitronekti-nos, fibronektin, kollagén és más fehérjék. Ing-tegriny képes felismerni egy jellegzetes S-sav-szekvencia RGD (TTI Tripepi-Arg-Gly-Asp), elérhető az ligandumok. Ez POS következetesen jelen van az összes adhéziós proteinek vérfehérjék # 945; -granul vérlemezke-FIB rhinogenous, von Willebrand faktor, fibronektin, vitronektin, laminin. Az újonnan-integráló vegyületek ligandumok jellemző függőséget dvuhva-vegyértékei kationok Ca 2+ és Mg 2+.
A komplex GPIIb-IIIa vérlemezke integrin receptor, amely létezik interakció, elsősorban a fibrinogén (fib-rinogenovy receptor). Ez a kölcsönhatás egy elsődleges útvonal vérlemezke-aggregáció-Ing egymással keresztül „fibrin hidak”. A veleszületett hiányossága ezen receptor -trombostenii Glantsmana - hirtelen törött vagy hiányzik vérlemezke-aggregációt a többségi-stvom aggregáció induktorok, ideértve a hívás-gén trombin ADP. A vérlemezke-aggregációt ezekkel induktorok, mint hiányzik a szenvedő páciensek afibrinogenemia ha fib-rinogen hiányzik is a vérlemezke tároló medencék magukat.
A komplex jelenléte a GP IIb-IIIa helyeken raspoz-RGD Navan magyarázza a képességét, az in-tegrina kapcsolódni a von Willebrand faktor, fibronektin. Az eredmények azt mutatják, hogy a kapcsolat GPIIb-IIIa von Willebrand faktor fontos a hatékony lévő vérlemezkék aggregációjának a feltétel-ditions hatását a magas áramlási sebességek. A legfontosabb jellemzője a komplex GPIIb-IIIa az a képesség, hogy végre a szerepe a receptor csak a felszínen aktivált trombózis tsitov. A affinitása e komplex a felső felületen nem-aktivált sejtek nagyon alacsony, és annak antigén jellemző eltér a-kovoy aktív vérlemezkék. A vérlemezkék aktiválódása jelentős magasabb niju antigén affinitás és a változás-it, azzal jellemezve GPIIb-IIIa.
Az aktivált vérlemezkék Vat kötőanyag a felületükön több mint 40.000 molekula fibrinogén útján GPIIb-IIIa. Ez a kölcsönhatás
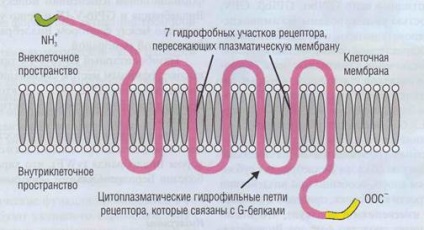
Ábra. 20. A trombin receptor a vérlemezke membrán receptorokhoz hasonló szerkezetű, hogy az ADP, adrenalin, szerotonin, eikozanoidok és egyéb kis molekulatömegű vegyületeket. Mivel a több hurkot a receptor a set-gofunktsionalny karakter. Az intracelluláris C-terminális kölcsönhatásba lép a cAMP-függő protein-kináz, receptor-WIDE hidrofil hurok aktiválásához G-protein által közvetített intracelluláris funkcionális változásokat. A Stora számunkra N-végén trombin okoz részleges proteolízissel, és így aktiválja a receptor
Ez történik a kétértékű kationok (Ca2 +) és a kezdetben reverzibilis. Továbbá, mivel a formáció további con-ciklusok történik stabilizáló egység.
25% -át a lakosság az észak-európai kapcsolatban on-allél polimorfizmus GPIIIa van szövetségeknek a szívkoszorúér-betegség és a szívizom INFAR-CTA viszonylag fiatal korban.
Inhibitorok használatával a GPIIb-IIIa komplex a korai szakaszában a trombózis vezet a gyors helyreállítása a véráramlás a véredényben Trom-szorbeált és elkerüli INFAR KTA-trombotizált testet.
Receptorok fiziológiás stimulánsok
Receptorok fiziológiai stimulyato-árok (trombin, ADP, adrenalin, szerotonin,
és más eikozanoidok.) transz-membrán hidrofób peptidek 7-rami ismétlődések, 7-szer, hogy átlépje a plazmamembrán (ábra. 20). Köztük nagy hidrofil rész kifelé és a sejtbe. A citoplazmatikus C-terminális lehet foszforilált proteinki-nazami elsősorban cAMP-dependens kina-Zoe. A citoplazmatikus hurkokat kötőhelyek egy G rendszer-fehérjék, amelyek intracelluláris mediátorok biztosították biztosítja, különböző fiziológiai rea-TION, különösen a belső-felszabadulásra kifejtett Ca 2+ medence. Az egyes aktivált bins Trom-receptor képződéséhez vezet a nem-hány intracelluláris messengerek acti-Adósságmegújítási vérlemezkék.
A citoplazmában a vérlemezkék elrendezett mitokondriumok, peroxiszóma (tartalmaznak kataláz-zu) befogadás glikogén, lizoszómák és granulátumok tartalmazó víztárolókban a különböző anyagok. Az izolált vérlemezkéket 3 féle organellumok Church a létesítmény: egy-granulátum, elektron-sűrű testek (8 pellet) és lizoszómák (y-granulátum). Ábra. A 21. ábrán a fő komponensek, amelyek felszabadul a szemcsékből és a citoszol Trom-botsitov hatására különböző stimulátorok.
Az A-tárolt granulátumok akár 30 különböző Br-nek, melyek többsége még HN sintezirova a megakariociták: # 946; -tromboglobulin, vérlemezke faktor 4, V-ös faktor Villeb-rand, fibrinogén, trombospondin, fibronek Ting, vitronektin, SC-makroglobulin, P-szelektin, vérlemezke-eredetű növekedési faktor (PDGF), egy inhibitor TCA-típusú plazminogén aktivátor nevogo 1 (PAI-1), # 945; 2-antiplazmin, # 945; 1-antitripszin, protein-S, a leukocita kemotaktikus faktor SZEZON molekulatömegű kininogén, stb részvétele bel-Ing. # 945; -granul kóros és fiziológiai folyamat többoldalú-CAL: a) a mitogén és kemotaktikus hatást; b) egy ragasztó akció, modulációs a vérlemezke-aggregáció; c) ESTATE távú vérzéscsillapítás a láng; g) vazoaktív dei következmény; d) immun-és egyéb hatások.
A sűrű testek (5-granulátum) vannak tárolva alállomás, ami elsősorban a vascularis válaszreakciók és vérlemezke-aggregáció: adenilsav
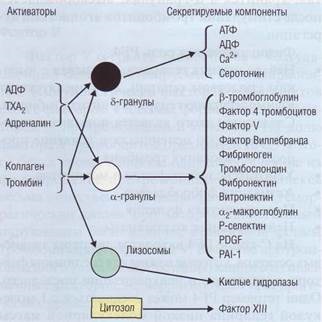
Ábra. 21. szekretált vériemezke faktorok pres-léteznek vérlemezkék 3 féle tárolási granulátumok. Egyéb stimulánsok kibocsátásához vezethet tartalmának gra nulla vérlemezkék
nukleotidok (ATP, ADP, AMP, c-AMP, GDP)
szerotonin, adrenalin, noradrenalin, dopamin, hisztamin, Ca 2+, stb kiszabadulnak a tároló medence az ATP és ADP-Xia gyorsan metabolizálódik a plazmában AMP és az adenozin .; az utolsó füstölő-Direct koronarorasshiryayuschee akció-enni. ADP egy kritikus élettani metabolit, így primer hemo stasis-vérlemezke aggregációt stimuláló.
A lizoszómák (# 947; -granuly) hidrolizáljuk-cal enzimek - peroxidáz, glükozidáz, galaktozidáz, vagy # 946; -glitserofosfataza, savas foszfatáz, a nem specifikus észteráz. Lizoszómák szekretálnak alatt a titkos csak a visszafordíthatatlan aktiválást.
A vérlemezkék képesek szekretálni-zhimoe tartalmaznak szemcsék részben reverzibilis, amikor AK-
tivatsii és a folyamat a trofikus kölcsönhatás szerv-ményeit a kapilláris hálózat, és a padló-ség által a reakció a felszabadulás társított irreverzíbilis aktiválása. „Elpusztult” után a citoplazmában vérlemezke degranulatiót. In-Neak-aktivált vérlemezkék citoplazma tűnhet „elpusztult” veleszületett de töltés granulátum, ami a DEFI-tsitu tároló medence - szindróma „szürke” tromboembóliás tsitov.
A szekréciót követően, a többség a granulált membrán lebomlik, a granulátumot nem helyreállítása, és a vérlemezkék elvesztik fiziologiches-kuyu aktivitást. Ha ezek a jelenlegi Cro-vie, egy módosított formáját hozzájárulva a gyors kiürülés a lépben.