Inert gázok - az
kémiai tulajdonságok
Inert gázok különböző kémiai inaktivitás (innen a név). Azonban, 1962-ben, Neil Barlett azt mutatták, hogy mindegyik képezhet vegyületet (különösen könnyen fluorid) bizonyos feltételek mellett. A legtöbb „inert” neon és hélium: hogy tudnak reagálni, meg kell alkalmazni a sok erőfeszítés mesterséges ionizáló minden atom. Xenon, Ezzel szemben, a túlzottan aktív (inert gáz), és reagálni, még normális körülmények között. bizonyítva szinte az összes lehetséges oxidációs állapotban (+1, +2, +4, +6, +8). Radon is magas kémiai aktivitással, de ez nagymértékben radioaktív és lebomlik gyorsan, így egy részletes tanulmányt annak kémiai tulajdonságai bonyolult, ellentétben a xenon. Ununoctium. annak ellenére, hogy csoportba tartozó 18 a periódusos rendszer, ez lehet inert gáz, mivel feltételezhető, hogy normál körülmények között befolyásolja a relativisztikus hatásokat, ez lesz a szilárd állapotban [2].
fizikai tulajdonságok
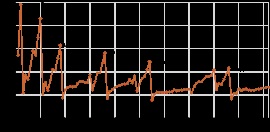
Az inert gázok legnagyobb ionizációs energia.
Inert gázok színtelenek és szagtalanok. Néhány ezek jelen vannak a levegőben, és a sziklák. valamint bizonyos környezetekben az óriás bolygók.
A biológiai hatás
Inert gázok nem toxikusak. Azonban, a légkör megnövekedett koncentrációja inert gáz és a megfelelő csökkenését oxigénkoncentráció hatással lehetnek az emberi fojtogató, egészen a eszméletvesztést és a halál [3] [4]. Ismert halálesetek argon alatt szivárog.
Inert gázok biológiai aktivitást mutatnak, amely abban nyilvánul meg, hogy narkotikus hatása van a szervezetben, és az erős ez a hatás azonban a következő sorrendben (az ábrán látható összehasonlítva nitrogén és hidrogén): Xe - Kr - Ar - N2 - H2 - Ne - Ő. Így xenon és kripton mutatnak gyógyszer hatását normál légköri nyomáson, argon - nyomáson nagyobb, mint 0,2 MPa. nitrogén - több, mint 0,6 MPa, a hidrogén - több, mint 2,0 MPa. Narkotikus hatásával neon és hélium nem regisztrált a kísérletekben, mint a nyomás, mielőtt a tünetek jelentkeznek „nagynyomású ideges szindróma” (NSVD) [5].
kérelem
Az inert gázok nagyon alacsony forráspontja és olvadáspontja, ami lehetővé teszi, hogy használja őket, mint a hűtőközeg kriogén mérnöki. Különösen a folyékony hélium. amelynek forráspontja 4,2 K (-268,95 ° C; -452,11 ° F), használjuk a mágneses szupravezetés, mellyel a mágneses rezonancia képalkotás és a nukleáris mágneses rezonancia. Folyékony neon bár nem éri el, mint alacsony hőmérsékleten, mint a folyékony hélium, amint használunk Kriogenikai, mert hűtési tulajdonságai több mint 40-szer nagyobb, mint a folyékony hélium és több mint háromszor nagyobb, mint a folyékony hidrogén.
Hélium használják légzési gáz komponensek (gáz keveréke) nitrogén helyett, mert az alacsony oldhatósága a testnedvekben, különösen a lipidek. A gázokat felszívódik a vér és a test szöveteiben. amikor nyomás alatt vannak, mint például a búvárkodás. ez az oka a hatás néven ismert nitrogén narkózis. Mivel kisebb oldhatósága, egy kis hélium késleltetett sejtmembrán. és ezért a hélium légzéshez használt keverékek, mint trimix és HELIOX. narkotikus hatása redukáló gázok felmerülő mélységben. Csökkentett oldhatósága hélium ad más előnyöket a ismert állapot dekompressziós betegség. Csökkentése a maradékot feloldjuk gázt a szervezetben azt jelenti, hogy kisebb mennyiségű gázt képződő buborékok emelkedés közben. Egyéb inert gáz, argon, tekinthető a legjobb választás használatra rétegként egy száraz ruha [6], búvár, valamint a nagy mennyiségű kezelésére használjuk a folyékony acél.
Miután összeomlott a léghajó Gindenburg 1937 hélium helyébe hidrogén, mint az emelő gáz léghajók és léggömbök miatt nonflammability és megkönnyítik annak ellenére, hogy a 8,6% -os csökkentése felhajtóerő (felhajtóerő).
jegyzetek
Ez a cikk nem illusztrációk.
Lásd, amit a „nemesgáz” más szótárak:
Inertgáz - (inert gázok; n Inertgase, Tragergase; f Gaz inertes; és gázok inertes ....) nemesgázok nemesgáz egyértékű színtelen és szagtalan: hélium (He), neon (Ne) ... Geológiai Encyclopedia
Inert gázok - (nemesgázok, nemesgáz) elemek Ch. alcsoportja a VIII csoportjába periodikus. A rendszer elemei. KI igaz volt hélium (He), neon (NE), argon (Ar), kripton (Kr), xenon (Xe) és a radioaktivitás. radon (Rn). A természetben, az AI a légkörben jelenlévő, nem ... ... Fizikai enciklopédia
Inert gázok - ugyanaz, mint a nemes gázok ... kollégiumi szótár
Inert gázok - ugyanaz, mint a nemes gázok ... Magyar Encyclopaedia of Occupational Safety
Inert gázok - inert gázok, ugyanaz, mint a nemesgázok. ... Illustrated Encyclopedic szótár
inert gázok - Elements periódusos rendszer VIII. Rendszer: Nem, Ne, Ar, Kr, Xe, Rn. I. különböző kémiai. tehetetlenség miatt stabil Ext. E-konstans borítékot egy raj nem a 2 e kapcsolva, a fennmaradó 8 új e-mail. AI-t jellemzi a magas potenciállal ... Referencia műszaki fordító
inert gázok - [inert gázok] elemeinek VIII csoportba a periódusos rendszer: Nem, Ne, Ar, Kr, Xe, Rn. Inert gázok különböző kémiai semlegesség, miatt a stabil külső elektron héj, amely nem a 2 elektront, a fennmaradó 8 ... ... Encyclopedic szótár kohászati
Inert gázok - nemesgáz, nemesgázok, a kémiai elemek alkotó fő alcsoportja a 8. csoport a periódusos rendszer: Hélium Ő (atomszámú 2) Neon Ne (10) Argon Ar (18) kripton Kr (36) Xenon Xe (54) és a radon Rn (86). A ... ... Nagy Szovjet Enciklopédia
Inert gázok - GROUP 0. nemesgáz (semleges) GÁZOK hélium, neon, argon, kripton, xenon, radon atomok elemei a nulla csoport teljesen kitöltött külső elektron héj, amely megfelel a legstabilabb elektronikus konfiguráció, és a ... ... Collier Encyclopedia
- Állítsa be a táblákat. Kémia. Nemfémek (18 táblázatok). Képzési album 18 lap. Art. 5-8688-018 halogének. halogénatom kémia. Kén. Allotrópia. kén kémia. Kénsav. Nitrogén Chemicals. Nitrogén-oxidok. Salétromsav - oxidálószer. Foszfor. ... Tovább Vásárlás 4176 rubelt
- Nemesgáz. Dzhessi Rassel. Ez a könyv lesz összhangban a rendelését Technology Print-on-Demand technológiát. High Quality Content Wikipedia cikket! Blagoro dnye gáz (szintén semleges vagy nemesgáz?) - ... Tovább Vásárlás 1125 rubelt
- Inert gázok. Dzhessi Rassel. Ez a könyv lesz összhangban a rendelését Technology Print-on-Demand technológiát. High Quality Content Wikipedia cikket! ? Ine rtnye vagy blagoro dnye gázok - kémiai elemek ... Tovább Vásárlás 998 rubelt