folyamat funkciók
Mivel a függvény az állam kötött állami egyenletek és egyéb egyenletek (például az egyenlet Gibbs - Duhem) egyértelmű jellemző a rendszer állapota elegendő tudni, csak a néhány változó nevű független állapotváltozók vagy rövidebben az állam paramétereket a termodinamikai rendszer. A többi állami funkció egy matematikai állapot függvényében paraméterek és egyedileg határozzák meg, amikor beállított tart. Ráadásul sok alkalmazás nem számít, hogy az ismert fajlagos állapotegyenlet a vizsgált rendszerrel; csak az fontos, hogy a megfelelő függően mindig igazán létezik. A számos állami paraméterek jellegétől függ az adott rendszer, és a választás önkényes, elvileg, és összefügg megfontolások célszerűségi. [1]
folyamat funkciók függnek nemcsak a jelenlegi állapotában a rendszer, hanem az, ahogyan a rendszer azért jött, hogy ezt az állapotot.
A funkciók a folyamat termodinamikai vonatkoznak
· Q hőmennyiség,
· A termodinamikai munkát.
A egyensúlyi folyamatok, ezek az értékek is kifejezhető az állam a funkciót integráló tényező:
· DS = # 948; QT. ahol S (entrópia) és a T (abszolút hőmérséklet) - a funkcióra
Nyomás - ez fizikai mennyiség, egyenlő az arány a merőleges komponense ható erő a felszínen a terület a felületre.
Erő hat a falhoz számos molekulák. Meg lehet kiszámítani a termék a kifejtett erő egyetlen molekula által, a molekulák száma mozog az edényben az irányt a fal. Mivel a tér három dimenziós, és mindegyik dimenziónak két irányban: pozitív és negatív, akkor feltételezhetjük, hogy az irányt egyik fal mozog egyhatoda összes molekulák (ha számuk nagy): N = N0 / 6.
A kifejtett erő a fal egyetlen molekula által, egyenlő a ható erő egy molekulában a faltól. A ható erő egy molekulában a fali egyenlő tömege alkalommal a gyorsulás egy molekula, amely nem lesz, amikor eltalál a fal:
Gyorsítás azonos - a fizikai mennyiség által meghatározott aránya az idő változás mértéke, amelynek során a változás: a = # 916; # 965; / T.
Speed változás kétszeresével egyenlő a molekula ütközési sebességet: # 916; # 965; = -2 # 965;.
Ha a molekula úgy viselkedik, mint egy gumilabda, nem nehéz elképzelni, hogy a hatás a folyamat: a molekula eltalálásáról deformálódott. A folyamat tömörítése és kicsomagolása töltött időt. Mindaddig, amíg a molekula hat az érfal, egy utolsó alkalommal, hogy elérje néhány molekulák száma azt távolságok belül L = # 965; t. (Például, viszonylag szerény, hagyja, hogy a molekulák egy sebessége 100 m / s. Beat tartós 0,01 másodpercig. Ezután erre az időre, hogy sikerül elérni a falra, és hozzájárulnak a nyomás a molekulák úgy távolságból 10, 50, 70 cm-es de belül 100 cm).
Úgy véljük, a kötet a hajó V = IS.
Behelyettesítve az összes képlet az eredeti, megkapjuk a következő egyenletet:
ahol: - a tömege egy molekula - átlagos négyzetes molekulák sebessége, N - molekulák száma a kötet V.
Tegyük néhány megjegyzést az egyik változót tartalmazza a kapott egyenlet.
Mivel a mozgás az molekulák és a preferenciális kaotikus mozgását molekulák az edényben nincs jelen, az átlagos sebesség egyenlő nullával. De nyilvánvaló, hogy ez nem vonatkozik minden egyes molekula.
Ahhoz, hogy kiszámítják az ideális gáz nyomása az edény falához használják nem jelenti azt, x értéke-komponenseinek a molekulák sebességét és az átlagos négyzetes sebesség
Ahhoz, hogy a bevezetése ez az érték inkább egyértelmű, nézzük egy számszerű példát.
Legyen négy molekula van egy sebesség 1, 2, 3, 4, konv. u
Szögletes átlagsebessége a molekulák:
Egyenletek makroparamétert kapcsolódó gázok - a nyomás és térfogat (p V.) A mikroparamétert - molekulák és azok sebessége (m0. # 965;), vagy az energia
Az utolsó egyenlet a következőképpen szól: ideális gáz nyomása az edény falához egyenesen arányos a molekulák koncentrációja az edényben és az átlagos kinetikus energia.
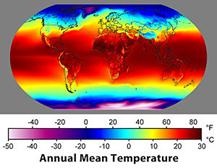
Az évi átlaghőmérséklet világszerte
hőmozgás # 945; peptidkomplexekre. Egy komplex oszciiiáiómozgásban alkotó atomok a peptid véletlen és az energia egyetlen atom ingadozik széles határok alkalmazásával ekvipartició törvény átlagából számítjuk kinetikus energia minden egyes atom, és az átlagos potenciális energiája sok ingadozások. Gray, piros és kék gömbök képviseli szénatomot, oxigén- iazota rendre; Kis fehér golyó hidrogénatomot jelent.
A nemzetközi rendszer egységek (Eng. Nemzetközi mennyiségrendszerben. ISQ) termodinamikai hőmérséklet választották az egyik a hét alapvető fizikai mennyiségek rendszer. Ennek megfelelően vMezhdunarodnoy rendszer (SI) mennyiségek alapján az International System, ez az egység hőmérséklet - Kelvin - egyike a hét alapvető SI egységeket. Emellett termodinamikai hőmérséklet Celsius hőmérséklet SI használt, mértékegysége Celsius fok, egy része a származtatott SI-egységek, amelyek speciális nevekkel és jelekkel, és a mérete megegyezik Kelvin [4]. A gyakorlatban, gyakran használják, hogy Celsius fok miatt fontos történelmi kötési jellemzőit a víz - az az olvadó jég hőmérsékletén (0 ° C) és a visszafolyatás hőmérsékletén (100 ° C). Ez kényelmes, mint a legtöbb éghajlati folyamatok, a természetben zajló folyamatok, és így tovább. E. Associated ezt a tartományt. A hőmérséklet-változás egy Celsius hőmérsékletet változtatni azonosan az egyik Kelvin. Ezért, 1967-ben bevezetése után egy új meghatározása Kelvin hőmérsékleten forró vízzel megszűnt, hogy szerepet játszanak állandó vonatkozási pont, és mennyire pontos mérések azt mutatják, hogy már nem egyenlő 100 ° C, és közel van a 99.975 ° C [2] .Van is Fahrenheit és mások.