Dehidrogenáz, egy szerkezetet és a cselekvés
Oxidációs szerves anyagok az élő szövetekben a növények és állatok történik részvételével enzimek dehidrogenáz - aktivátorok és hidrogén töltéshordozók (elektronok) és a légzés anyag oxidázok - aktivátorok a molekuláris oxigén.
Dehidrogenáz (a de novolat és hudrogenium - .. Hidrogén), enzimek, amelyek katalizálják a hasítási hidrogén szerves anyagoktól. D. koenzim általában dinukleotidokat:
- nikotinamid-adenin-dinukleotid (NADH) vagy flavin-adenin-dinukleotid (FAD)
- flavin-mononukleotid (FMN), amely elfogadja a hidrogén oxidálható anyagok. D. végzett első szakasza biooxidation.
Ők játszanak nagy szerepet a Krebs-ciklus glikolízis és pentózfoszfát ciklust. D. Egyes nem koenzimek, anyagok katalizálják az oxidációs reakciót közvetlenül oxigénnel. A legtöbb DA részeként az aktív centrum tartalmazza fémek - cink, mangán.
Dehidrogenáz működik az egész légzési folyamat, valamint a tevékenységek jellege oszlanak aerob és anaerob. Első transzfer hidrogén közvetlenül molekuláris oxigént, és a második -, hogy egy hidrogén-akceptor. Dehidrogenáz enzimek tartoznak a kétkomponensű - proteidek piridinnel és flavin (alloksazinovymi) koenzimek.
Piridint dehidrogenázok egy csoportja anaerob dehidrogenázok, amelyek hidrogén-akceptor szubsztrát. Specifitását ezek az intézkedések a képessége hidrogénezést és dehidrogénezést piridin magok.
Ábra. 1 - Piridin
Azáltal flavoproteidnym dehidrogenázok közé tartoznak az enzimek, amelyek összetétele riboflavin-foszfát-észter.
Ábra. 2 - Riboflavin
2. Nikolaev A. Ya. Biological Chemistry. M High School, 1989, pp 199-221.
5. Lehninger A. Fundamentals of Biochemistry. Mir, 1985. T. 2. S. 403-438, 508-550.
7. Skulachev VP biologicheskihmembran energiát. M. Science. 1989.
8. Ez egy folyamat oxigén fogyasztása sejtek a test szöveteiben, amely részt vesz a biológiai oxidáció. Ez a fajta oxidáció hívják aerob oxidáció. Ha nem a végleges akceptor oxigént működik, mint egy hidrogén-transzfer áramkört, és egyéb anyagok (például piroszőlősavat), egy ilyen típus az úgynevezett anaerob oxidáció.
9. Így biológiai oxidáció - egy dehidrogénezési szubsztrát alkalmazásával köztes vektorok hidrogén és a végső akceptor. A biológiai oxidáció tápanyagok zajlik a mitokondrium. Ők mutattak részt vevő enzimeket a citromsav-ciklus, a légzési lánc, az oxidatív foszforiláció, a hasítási zsírsavak és néhány aminosavat.
10. A légzési lánc (enzimekkel szöveti légzést) - a proton és elektron-hordozóként az oxidálható szubsztrát oxigént. Az oxidálószer - egy vegyület, amely képes elfogadni elektronokat. Ez a képesség, mennyiségileg az oxidációs-redukciós potenciál viszonyítva a standard hidrogén elektród, a pH egyenlő 7,0. Minél alacsonyabb a potenciálja a vegyület, annál erősebb a redukáló tulajdonságai, és fordítva.
11. jellemzők szöveti légzés
12. A folyamat a szöveti légzést nem tekinthető azonosnak biooxidation processzeket (enzimatikus oxidációját különböző szubsztrátok, előforduló állati, növényi és mikroorganizmus-sejteket), mivel egy jelentős része az ilyen oxidatív átalakítások a szervezetben fordul elő, anaerob körülmények között, azaz a részvétele nélkül a molekuláris oxigén, szemben a légúti szövetek.
A legtöbb energia aerob sejtekben keresztül szöveti légzést és termelt energia mennyisége függ az intenzitása. . D. intenzitása t meghatároztuk az oxigén felvétel arányának egységnyi tömegű szövet; általában annak köszönhető, hogy az energia- szövetet. A támogatás intenzitása a legmagasabb a retina, vese, máj, hogy jelentős a bél nyálkahártyájában, a pajzsmirigy, a herék, agykéreg, agyalapi mirigyben, a lépben, csontvelőben, tüdőben, méhlepényben, a csecsemőmirigy, a hasnyálmirigy, a rekeszizom, szívben, vázizomban, található, a nyugalmi állapotban. A bőr, szaruhártya és a szemlencse a szem szöveteit légzés aránya alacsony. Pajzsmirigy hormonok, zsírsavak és más biológiailag aktív anyagokkal aktiválhatjuk szöveti légzést.
Az intenzitás ilyen légzőszervi meghatározott polarográfiásan vagy manometrikus Eljárás egy Warburg berendezésben. Az utóbbi esetben jellemzésére használt az úgynevezett légzési hányados - aránya a keletkezett szén-dioxid-gáz térfogatának abszorbeált oxigén egy bizonyos mennyiségű a szövet idővel.
13. Így. bármilyen vegyület lehet adományozni elektronok csak egy vegyület egy nagyobb redox potenciál. Minden ezt követő légzési láncszem van egy nagyobb potenciállal rendelkezik, mint az előzőt.
14. A légzési lánc
15. A légzési lánc áll NAD - függő dehidrogenázok; FAD- függő dehidrogenáz; Ubikinon (KoQ); Tsitohrmov b, c, a + a3.
16. NAD-függő dehidrogenáz. Mivel a koenzim például a NAD és NADP. A nikotinamid piridingyűrű kapcsolni képes a hidrogén-protonok és elektronok.
17. FAD és FMN-függő dehidrogenáz koenzim tartalmazzák, mint a foszfor-észter-vitamin B2 (FAD).
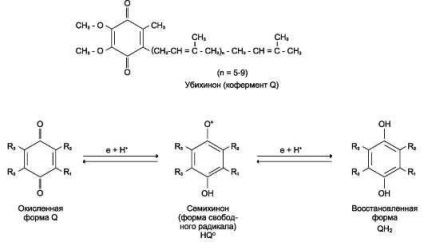
18. ubikinon (KoQ) veszi hidrogén flavoproteinek és alakítjuk hidrokinon.
19. citokróm - chromoproteids fehérjék kapcsolni képes elektronok jelenléte miatt az összetételét, mint prosztetikus csoportok ferroprotoporphyrin. Vesznek egy elektront egy anyag, ami egy kicsit a Bole erős redukálószer, és adja át a erősebb oxidálószer. Vas atom kapcsolódik a nitrogénatomhoz az imidazolgyűrű a hisztidin aminosav-maradékot ugyanazon az oldalon a porfirin a gyűrű síkjával, és másrészt a kénatommal metionin. Ezért a potenciális képességét, a vas atom a citokrómok oxigénkötő elnyomott.
20. citokróm c porfirin síkban kovalensen keresztül fehérjéhez kapcsolódó két cisztein csoport, és a citokrómok b, és egy, ez nem kovalens kötéssel kapcsolódik a fehérjéhez.
21. citokróm egy A3 + (citokróm-oxidáz) helyett tartalmazhatnak porfirin protoporfirin Egy eltérő számos szerkezeti jellemzők. Ötödik koordináció által elfoglalt amino vas tartozó aminocukor maradékot alkotó fehérje is.
22. Ezzel szemben a hem vas atom gemolgobina citokrómok is reverzibilisen váltani egy két vegyértékű állapotba ez biztosítja a közlekedési elektronok.
23. A szöveti oxigén igény és készletek
Tissue oxigénigény függ a funkcionális állapotban a sejtek szerkezetén belül. oxigénfogyasztás sebesség jellemzően milliliterben oxigén per 1 g tömegű percenként. Nyugalmi, az oxigén felszívódik viszonylag gyorsan a szívizomban, agy, szürkeállomány (különösen az agykéregben), a máj és a vese kortikális anyag. Ugyanakkor, vázizom, lép és fehérállomány az agy önmagában keveset fogyaszt oxigént.
By aktivitásának növelésével egy szerv szükség van rá az oxigén növekszik. Amikor megterhelés miokardiális oxigénfogyasztást növelheti 3 - 4-szer, és a munka vázizmok - több, mint 20 - 50-szer többi részéhez képest. Oxigén fogyasztás vesék növekszik az intenzitása a reabszorpciója nátrium ionok.
Oxigénhiányos szövetek
NADH dehidrogenáz tartalmaz több központ Fe2 S2 típusú és FE4 S4. A vas-atomok az ilyen központok, de elfogadja és adományozni elektronok viszont, átadva a ferro (Fe 2+) és ferri-(Fe 3+) állapotban. A vas-kén központok elektronok átkerülnek a koenzim Q (ubikinon) (ábra.).